Système de santé
Qu’est-ce qui rend les médicaments si coûteux?
Archive · 20 novembre 2019

En début d’année, Madame C. s’est vu diagnostiquer un cancer du système digestif. Son oncologue lui prescrit alors un traitement comportant un principe actif, l’imatinib, particulièrement efficace pour son type de tumeur. Les propriétés de cette molécule et, surtout, la gestion de son brevet vont la confronter à une situation kafkaïenne.
Patiente prise en otage
L’imatinib a été commercialisé en 2001 sous le nom de Glivec® pour le traitement d’une forme spécifique de leucémie. Il s’est avéré particulièrement efficace, mais aussi très lucratif pour Novartis qui en détient le brevet, générant, en 2013, un chiffre d’affaires mondial de près de 4,7 milliards de dollars. Le brevet a échu en 2016, permettant l’apparition d’un générique. Après son lancement, on lui a découvert une très bonne efficacité thérapeutique contre certains types de cancer digestif. Mais entretemps, pour l’indication spécifique de ce cancer, le fabricant a obtenu une prolongation de son brevet, toujours en vigueur.
Revenons à Madame C. Elle se rend chez son pharmacien et apprend l’existence du générique du Glivec®, forcément moins cher. On parle d’un montant de 17 000 fr. contre 35 800 fr. par an à posologie standard. Sensible à la problématique des coûts de la santé, Madame C. opte pour le générique. Sa caisse lui rembourse sans sourciller la première tranche de traitement. A la deuxième série de factures, en revanche, elle l’avertit que le générique ne peut être remboursé par l’assurance de base puisqu’il n’est pas homologué pour le cancer dont elle souffre… La caisse ne respecterait pas les clauses légales si elle s’exécutait. Elle lui présente alors une ardoise de près de 4000 fr. et lui indique qu’elle doit opter pour l’original même s’il est plus cher.
Une caisse qui demande à payer un traitement plus cher et une patiente qui doit payer davantage que si elle avait recouru au traitement le plus coûteux? Cette situation absurde affaiblit la promotion des génériques, mesure phare pour abaisser les coûts de la santé. Elle résulte surtout du jeu des brevets et du fait que, hormis son détenteur, personne n’est susceptible d’en modifier le périmètre ou les règles.
Opacité et manque d’information
En 2010, les dépenses pour les médicaments s’élevaient à 693 fr. par habitant. En 2017, ce chiffre atteint 814 fr. En l’espace de sept ans, le résidant suisse moyen a donc augmenté ses dépenses de 17,5%. A une autre échelle, les médicaments représentent environ 20% des remboursements effectués par l’assurance obligatoire. La baisse des prix des médicaments constitue donc un des leviers importants pour stopper la hausse des primes.
La mesure paraît simple dans un pays où les génériques coûtent en moyenne le double des prix pratiqués à l’étranger, et où les médicaments sous brevet continuent à être plus chers qu’ailleurs (voir infographie ci-dessous). De leur côté, Novartis et Roche ont beau être des fleurons suisses, ces pharmas ne semblent pas vouloir accorder de préférence au marché helvétique. Le Lucentis® (Novartis), utilisé pour le traitement des troubles de la vue, est moins cher respectivement de 29% en Belgique, de 38% en France et de 22% aux Pays-Bas. Ces derniers paient même 84% moins cher le Gilenya® (Novartis), utile dans le traitement de la sclérose en plaques (source: Curafutura-SASIS).
Pour Cécile Rivière, responsable romande d’Interpharma, «le prix des médicaments est défini par la loi et il n’existe pas de mécanisme de préférence nationale pas plus pour les médicaments que pour d’autres biens et services qu’on associerait à la Suisse, comme l’horlogerie, le chocolat ou le fromage. L’industrie pharmaceutique contribue fortement à la prospérité du pays grâce aux emplois créés, aux investissements dans le domaine de la recherche en Suisse.» Pourtant, au niveau mondial, le marché helvétique ne représente guère plus de 1% du volume des ventes. Malheureusement, fondé sur la plus-value vitale des médicaments que l’on ne trouve ni dans le fromage ni sur le cadran d’une montre, le système de fixation des prix complique considérablement les choses. Il est non seulement complexe, il est surtout opaque.
Importante marge d’économie
Après avoir été autorisé à la vente par Swissmedic, le succès commercial d’un médicament dépend de la décision de son remboursement par l’assurance obligatoire. A cette fin, les fabricants doivent fournir à l’Office fédéral de la santé publique (OFSP) une suite d’informations au sujet du médicament (sur son adéquation ou son économicité) et proposer un prix de remboursement. Le dossier est ensuite transmis à la Commission fédérale des médicaments (CFM, qui réunit des représentants des pharmas, des assureurs, des assurés, des pharmaciens et des médecins). Cette dernière évalue la conformité des données suivant deux critères: le bénéfice thérapeutique qu’elle compare avec les médicaments déjà sur le marché et les prix de référence pratiqués dans neuf pays européens.
Les évaluations de la CFM n’ont qu’un statut consultatif. L’Office fédéral de la santé publique est libre de mener ses propres négociations avec les fabricants. Les chiffres sur les investissements consentis pour le développement du produit sont non vérifiables. Enfin, les prix de référence sont souvent des prix vitrines. Ils ne tiennent pas compte des rabais octroyés par l’industrie qu’elle exige de ne pas divulguer sous peine d’y renoncer. De ce long processus rien ne filtre, si ce n’est le prix final… L’OFSP publie en ligne (et exclusivement en allemand) un compte rendu de ses évaluations. Leur contenu s’avère souvent trop synthétique. Par ailleurs, l’OFSP examine annuellement le prix d’une partie des médicaments remboursés par l’assurance obligatoire à des fins d’ajustement. Selon les chiffres annoncés par le Conseil fédéral, cette mesure a permis d’économiser depuis 2017 près de 450 millions. Malgré l’ampleur de la somme, la marge de progression demeure importante en Suisse.
MÉDICAMENTS BREVETÉS: DES ÉCARTS MARQUANTS
Comparaison des prix entre la Suisse et les pays européens de deux produits phares. L’anticoagulant Xarelto (Bayer) a généré le plus grand chiffre d’affaires (115 mio en 2017 et 127 mio en 2018) en Suisse. L’Humira (Abbvie), qui traite la polyarthrite rhumatoïde, suit juste derrière (105 mio en 2017 et 118 mio en 2018).
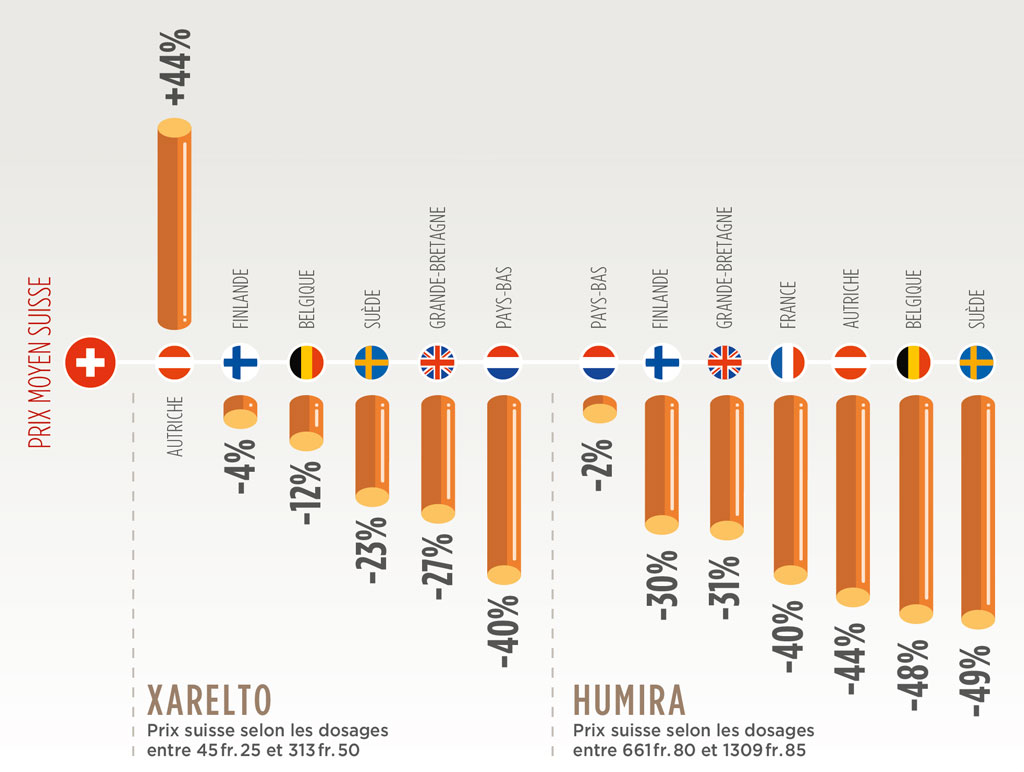
(source: Curafutura-SASIS)
Recherche: une saine concurrence
A la vue des montants nécessaires à l’invention d’un médicament et à sa mise sur le marché, il ne serait pas possible de faire sans les entreprises. Pour Interpharma, «le développement d’un médicament est une activité très dynamique, hautement compétitive et risquée. Il faut environ dix à quinze ans et des investissements considérables pour en développer un.
Neuf molécules ou produits sur dix, testés dans le cadre d’essais cliniques, échouent dans la toute dernière phase.» S’il est vrai que les fabricants sont actuellement les seuls dotés de l’infrastructure pour porter une telle démarche, ils n’assument pas les risques individuellement, voire ils les externalisent: Roche a ainsi acheté à coup de milliards des start-up ayant supporté les risques, et l’ONG Public Eye s’est récemment opposée à la demande de brevet pour un anticancéreux, le Kymriah, dont le développement doit beaucoup à des fonds publics de recherche. Sur un autre plan, l’industrie pharmaceutique cible ses investissements sur des secteurs rentables. Pour des domaines moins lucratifs et néanmoins nécessaires, les fonds publics jouent un rôle déterminant. Par exemple, la Confédération a déjà financé deux programmes nationaux de recherche en matière d’antibiorésistance pour tenter de juguler le phénomène.
Le Canton de Vaud, en partenariat avec la Fondation Ludwig, contribue largement au financement de traitements en immunologie oncologique.
Il se dit déjà que le prix de ces traitements sera fixé en fonction des coûts réels de recherche. Nous avons vérifié auprès du CHUV et la réponse s’avère laconique: «L’institution ne peut pas s’exprimer sur les conditions d’une éventuelle commercialisation de traitements qui en sont encore au stade des essais cliniques.» Une saine compétition entre les secteurs public et privé pourrait pourtant conduire à ramener le prix des traitements à des niveaux plus raisonnables. Le chemin est malheureusement encore long.
Enjeu: l’innovation en question
Trop peu de nouveaux traitements apportent un réel bénéfice thérapeutique. Comment renverser la tendance ?
Les hôpitaux disposent d’une certaine marge de manoeuvre pour obtenir des rabais, en particulier sur des traitements pour lesquels il existe plusieurs produits génériques. Thierry Buclin, médecin-chef au service de pharmacologie clinique du CHUV, confirme: «On essaie de limiter les dépenses grâce à ces négociations qui sont lancées dans le cadre d’un appel d’offres. Le fabricant qui fait la meilleure offre gagne, à condition que ce soit à caractéristique thérapeutique équivalente. Si ce n’est pas le cas, on pondère.» Les rabais obtenus sont en moyenne de l’ordre de 5 à 7% sur l’ensemble des médicaments hospitaliers. Même son de cloche du côté des cliniques privées: «Nous obtenons de très bonnes conditions lorsqu’il y a concurrence entre deux laboratoires», assure Zeynep Ersan Berdoz, responsable de la communication du groupe Aevis.
Ce type de négociation a ses limites. Si un médicament est le seul à traiter une pathologie ou s’il est plus efficace que tous les autres, il est à peu près impossible d’obtenir un rabais. Autrement dit, la marge des hôpitaux et des cliniques n’est pas la même selon qu’il s’agit de négocier le prix du paracétamol ou celui d’un traitement oncologique. En conséquence, un des enjeux centraux dans la fixation des prix consiste à définir le degré d’innovation des nouveaux traitements. Selon Dimitri Kohler, collaborateur scientifique à la Ligue suisse contre le cancer, «si certains traitements anticancéreux se sont révélés révolutionnaires au cours des dernières années, ce n’est pas le cas de tous les nouveaux médicaments mis sur le marché. On observe une tendance au développement de me too drugs, ou médicaments d’imitation. Ces derniers ont l’avantage d’assurer une bonne rentabilité à l’entreprise pharmaceutique ainsi qu’à ses actionnaires tout en limitant les risques inhérents au développement de médicaments plus révolutionnaires.» Plus largement, dans une étude récente, l’Institut pour la qualité et l’efficacité en soins de santé de Cologne estime que moins de 15% des traitements arrivant sur le marché apportent un réel bénéfice thérapeutique.
Appel à plus de transparence
Une solution serait de définir de façon plus stricte l’innovation et, de la sorte, être plus sévère lors de la mise sur le marché de médicaments. Plus facile à dire qu’à faire: d’une part parce que, pour que cette mesure soit vraiment efficace, il faudrait pouvoir accéder à toutes les données cliniques et pré-cliniques liées à un nouveau produit. Or, comme le constate Dimitri Kohler, il y a «une certaine opacité dans ces données et ces processus (…). Certains traitements peuvent alors paraître plus efficaces qu’ils ne le seront sur les patients qui y auront recours.»
D’autre part, Thierry Buclin rappelle que l’innovation n’est pas linéaire: «La vraie innovation se cache dans la fausse. Même les plus grands spécialistes n’ont pas tout juste en la matière. Par exemple, des petits détails paraissant insignifiants au départ peuvent, à l’usage, représenter de réelles avancées.» Une meilleure transparence quant à l’origine et à la qualité de données de recherche est une condition de base pour limiter l’incertitude, prendre les bonnes décisions et autoriser les traitements utiles aux patients.
UNE EFFICACITÉ PEU DÉMONTRÉE
Depuis 2015, sur 69 nouveaux médicaments évalués par l’Institut pour la qualité et l’efficacité en soins de santé de Cologne – toutes thérapeutiques confondues –, 9 apportent une réelle plus-value par rapport à ceux qu’ils remplacent.
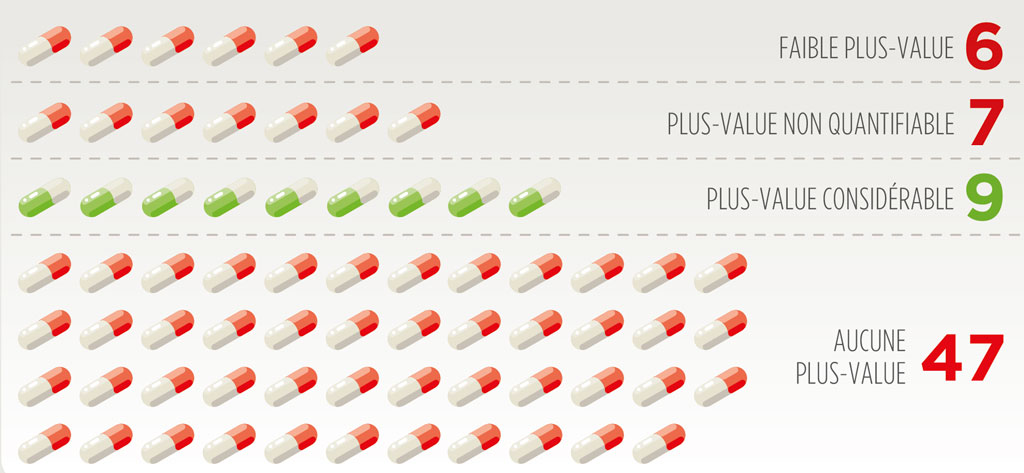
(source: Saldo)
Mieux se défendre: cinq mesures pour lesquelles plaide la FRC
RECHERCHE ET DÉVELOPPEMENT | Contraindre à une publication officielle et détaillée des montants liés à ce pan d’activité. Lors de la précédente assemblée générale de l’OMS, la Suisse a fait partie des pays qui ont freiné une résolution allant dans ce sens.
PRIX DE RÉFÉRENCE | Introduire ce prix pour les génériques puis, à terme, l’élargir à l’ensemble des médicaments ayant la même indication, qu’ils soient génériques ou originaux.
SURVEILLANCE | Autoriser Swissmedic à corriger les homologations lacunaires induisant un gaspillage de ressources (lire FRC Mieux choisir N°120, cas du Velcade). La France autorise par exemple son agence nationale de surveillance des médicaments à le faire.
IMPORTATION PARALLÈLE | Laisser la possibilité de s’approvisionner dans l’Union européenne au moins de façon transitoire pour autant que les standards en matière de sécurité soient respectés.
CONSOMM’ACTION | Les patients ont leur rôle à jouer en questionnant le bien-fondé d’un traitement et en n’hésitant pas à interpeller médecin ou pharmacien (voir carte «5 questions à poser à son médecin» jointe à cette édition).
AGIR
SOUTENEZ NOS ENQUÊTES. ON S'OCCUPE DU RESTE.
Preuves à l'appui, la FRC provoque des changements concrets. Faites un don.


Continuer ma lecture

Poker Menteur
Prouvé par la science: vraiment?

Cosmétiques
Choisir la meilleure crème solaire











